类器官一站式解决方案
类器官培养基试剂盒、类器官构建服务、类器官技术平台搭建服务
类器官药敏检测服务、CRO药效、安全性评估服务、类器官基因编辑服务等

2025年4月12日,发表在Nature Communications上的题为“Gut commensal Bifidobacterium-derived extracellular vesicles modulate the therapeuticeffectsofanti-PD-1inlungcancer”研究探讨了肠道共生菌双歧杆菌(Bifidobacterium)分泌的细胞外囊泡(Bifidobacterium-derived extracellular vesicles, Bif.BEVs)如何调节抗PD-1免疫疗法在非小细胞肺癌(NSCLC)中的治疗效果。

研究结果
研究目的
关键实验设计与方法
1.模型构建:
2.主要处理组:
1.Bif.BEVs调节免疫检查点表达:
实验表明,Bif.BEVs可以通过TLR4-NF-κB信号通路显著上调PD-L1的表达(图2d和图2e)。这一机制解释了Bif.BEVs如何影响肿瘤微环境,进而增强抗PD-1治疗的效果。
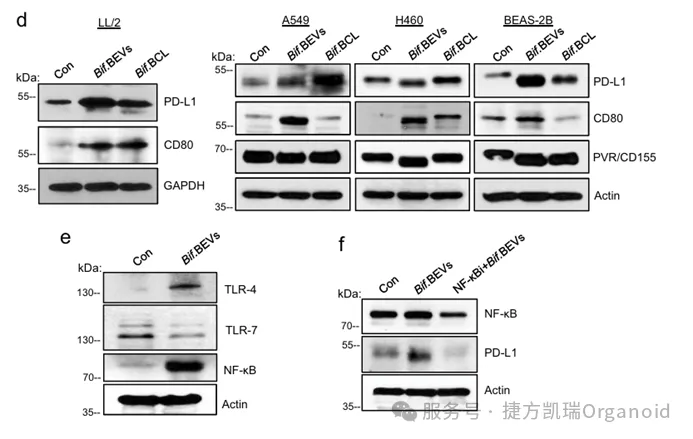
2.Bif.BEVs增强抗PD-1治疗效果
实验结果显示,口服给予Bif.BEVs(双歧杆菌来源的细胞外囊泡)能够显著增强抗PD-1免疫治疗在小鼠模型中的疗效。具体表现为,在LL/2肿瘤模型中,抗PD-1加Bif.BEVs(2 × 10^10)组的肿瘤生长明显减缓,肿瘤体积和重量显著低于对照组(图4b和图4c)。
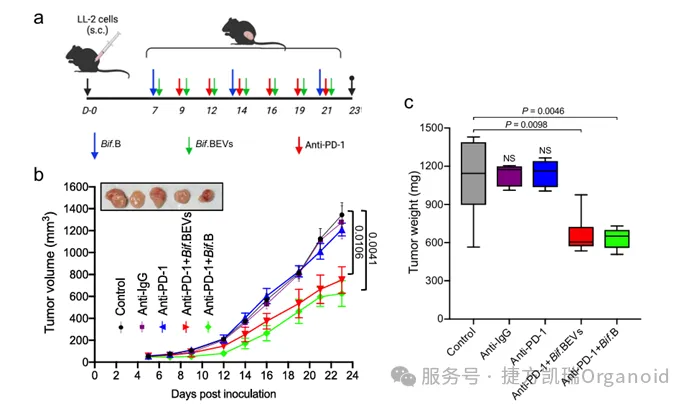
此外,抗PD-1加Bif.BEVs(2 × 10^11)组进一步增强了这种效果,肿瘤体积和重量显著降低(图4e和图4f)。这些结果验证了研究的假设,即Bif.BEVs可以提高抗PD-1治疗的效果。
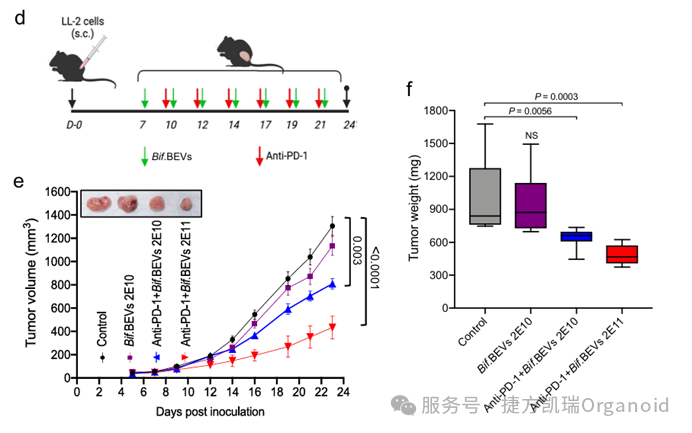
本文研究了肠道共生双歧杆菌来源的胞外囊泡(Bif.BEVs)对非小细胞肺癌(NSCLC)免疫治疗的影响。研究表明,Bif.BEVs可以通过上调PD-L1表达并增强抗PD-1的免疫治疗效果,显著改善NSCLC的治疗效果。虽然研究主要基于动物模型和体外实验,但其结果为未来临床应用提供了重要线索,特别是关于如何通过调节肠道微生物群来优化免疫治疗效果。未来需要更多的临床试验来验证这些发现,并进一步探索Bif.BEVs在其他癌症中的应用潜力。
1.诊断:
研究结果提示,检测患者肠道微生物群中的双歧杆菌水平可能有助于预测其对抗PD-1免疫治疗的反应。
2.治疗:
Bif.BEVs作为一种潜在的辅助治疗手段,可以与抗PD-1联合使用以提高治疗效果。此外,Bif.BEVs的剂量效应显示,更高剂量的Bif.BEVs可能带来更强的抗肿瘤效果。
3.预防:
通过调整肠道微生物群,特别是增加双歧杆菌的数量,可能会降低某些癌症的发生风险或改善免疫治疗的效果。
捷方凯瑞有成熟的肠类器官,肺类器官和肺癌类器官试剂盒,欢迎咨询交流!
扫描二维码关注:

联系销售
17749725176
lichangjie@jfkrorganoid.com
建议反馈
17749725176
您的每一条建议声音,我们都认真对待 7*24服务